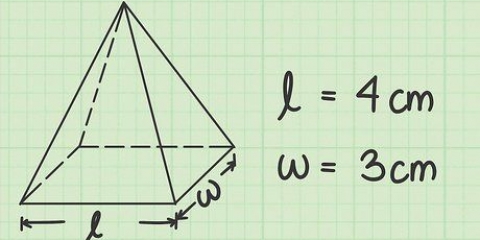Die Molmasse eines Elements ist also gleich der Molmasse eines Atoms mal der Anzahl der Atome in jedem Molekül: für Wasserstoff 1,008 mal 2 oder 2,016 Gramm pro Mol; Sauerstoff 15,9994 mal 2 oder 31,9988 Gramm pro Mol; und für Chlor 35,453 mal 2 oder 70,096 Gramm pro Mol. 

Die Molmasse jedes Elements von Chlorwasserstoff, HCl, beträgt 1,008 Gramm pro Mol Wasserstoff und 35,453 Gramm pro Mol Chlor. Die Molmasse jedes Glukoseelements, C6huh12Ö6, ist 12,0107 mal 6 oder 72,0642 Gramm pro Mol Kohlenstoff; 1,008 mal 12 oder 12,096 Gramm pro Mol Wasserstoff; und 15,9994 mal 6 oder 95,9964 Gramm pro Mol Sauerstoff. 
Die Molmasse von Chlorwasserstoff beträgt 1,008 + 35,453 oder 36,461 Gramm pro mol. Die Molmasse von Glucose beträgt 72,0642 + 12,096 + 95,9964 oder 180,1566 Gramm pro Mol.
Berechnung der molmasse
Atome sind zu klein für aussagekräftige Chemikalienmessungen. Um mit sehr geringen Mengen einer bestimmten Substanz arbeiten zu können, werden diese von Wissenschaftlern in Einheiten von mol . eingeteilt. Ein Mol ist definiert als eine bestimmte Stoffmenge mit so vielen Partikeln wie die Anzahl der Kohlenstoffatome in 12 Gramm des C-12-Isotops, was ungefähr 6.022 14 × 10 . entspricht. Dies wird die Zahl oder Konstante von Avogadro . genannt. Es wird verwendet, um die Anzahl der Atome, Moleküle, Ionen oder subatomaren Partikel in einer Substanz anzugeben, und die Masse von 1 Mol ist die Molmasse dieser Substanz. Lesen Sie hier, wie Sie die Molmasse von Elementen und Stoffen berechnen.
Schritte
Methode 1 von 2: Berechnung der Molmasse eines Elements

1. Finden Sie die relative Atommasse des Elements. Die relative Atommasse eines Elements ist der gewichtete Durchschnitt der Atommassen aller natürlich vorkommenden Isotope, ausgedrückt in Atommasseneinheiten (u).Sie finden diese Informationen im Periodensystem. Wasserstoff hat beispielsweise eine relative Atommasse von 1,008; Kohlenstoff 12.0107; Sauerstoff 15,9994; und Chlor 35.453.

2. Mit der Molmasse multiplizieren. Dies ist definiert als 1 Gramm pro Mol. Dies wandelt die atomare Masseneinheit in Gramm pro Mol um, wodurch die Molmasse von Wasserstoff 1,008 Gramm pro Mol, Kohlenstoff 12,0107 Gramm pro Mol, Sauerstoff 15,9994 Gramm pro Mol und Chlor 35,453 Gramm pro Mol beträgt.
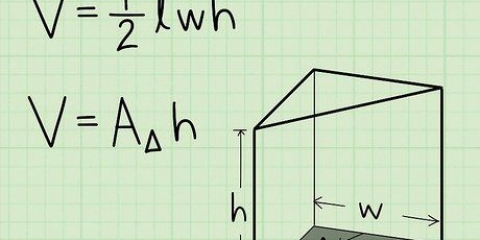
3. Finden Sie die Molmasse eines zweiwertigen Moleküls. Einige Elemente können nur in Molekülen von 2 oder mehr gefunden werden. Das heißt, wenn Sie die Molmasse eines Elements berechnen möchten, das beispielsweise aus 2 Atomen besteht, wie Wasserstoff, Sauerstoff und Chlor, die relative Atommasse bestimmen und mit der Molmasse multiplizieren und multiplizieren das Ergebnis um 2.
Methode 2 von 2: Berechnung der Molmasse einer Verbindung

1. Bestimmen Sie die chemische Formel der Verbindung. Dies ist die Anzahl der Atome in jedem Element der Verbindung. (Informationen dazu finden sich zB in den Binas) Beispiel: Die Formel für Chlorwasserstoff (Salzsäure) ist HCl; für Glucose C6huh12Ö6. Die letzte Formel bedeutet, dass Glucose 6 Kohlenstoffatome, 12 Wasserstoffatome und 6 Sauerstoffatome enthält.

2. Bestimmen Sie die Molmasse jedes Elements in der Verbindung. Multiplizieren Sie die Atommasse des Elements mit der Molmasse und der Anzahl der Atome des Elements in der Verbindung. So funktioniert das:

3. Addiere die Molmassen jedes Elements in der Verbindung. Daraus ergibt sich die Molmasse der Verbindung. So geht`s:
Tipps
- Während relative Atommassen in den meisten Fällen eine Genauigkeit von 4 Dezimalstellen haben, gilt im Labor eine Genauigkeit von 2 Dezimalstellen oder weniger für außergewöhnlich große Massen. Im Labor beträgt die Molmasse von Chlorwasserstoff also 36,46 Gramm pro Mol und die von Glucose 180,16 Gramm pro Mol.
Warnungen
- Molmasse und Molekularmasse nicht verwechseln. Letzteres ist die Masse eines einzelnen Moleküls eines Elements oder einer Verbindung. Unter Molmasse kann man die durchschnittliche Masse aller Moleküle in einer Probe einer bestimmten Substanz verstehen, ebenso wie die relative Atommasse der Durchschnitt der Atommassen aller Isotope ist.
Notwendigkeiten
- Binas und Periodensystem der Elemente
- Taschenrechner
Оцените, пожалуйста статью